欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
盐酸二甲双胍片的一致性评价资料
原研药学信息综述
国内上市情况
目前国内二甲双胍片(素片和薄膜衣片)有近100个文号,有0.25g、0.5g和0.85g几种规格。
有进口药品上市,H20140534,迪化唐锭,0.5g,Alphapharm Pty Limited; 有进口本地化产品上市,国药准字H20023371和国药准字H20023370,格华止,0.5g和0.85g,中美上海施贵宝制药有限公司;国药准字H20013054,0.25g,山德士(中国)制药有限公司。
国外上市情况
二甲双胍于1958年最早在英国上市,由一个叫Rona的公司销售。加拿大在1972年上市,FDA1994年12月批准施贵宝制药有限公司生产的盐酸二甲双胍片(Glucophage)在美国上市。
二甲双胍目前在全球多个国家上市,有多个商品名。
参比制剂
FDA橙皮书中参比制剂为施贵宝的GLUCOPHAGE,规格为1g。 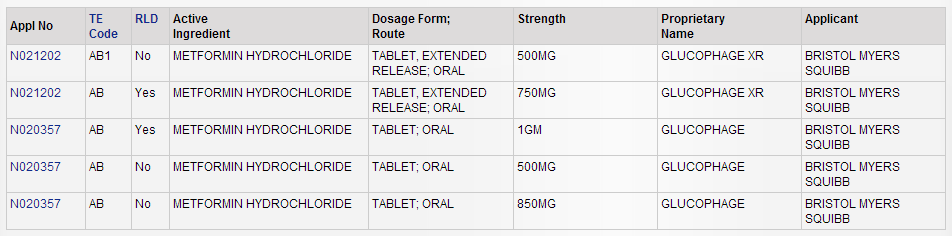
日本橙皮书中参比制剂为日本新药生产,规格250mg。 
原料药理化性质
解离常数:pKa=12.4(针对仲氨基)
在各pH值溶出介质中的溶解度(37℃): pH1.2:333mg/ml pH4.0:353mg/ml pH6.8:355mg/ml 水:346mg/ml
在各溶出介质中的稳定性: 水:未测定。 在各pH值溶出介质中:未测定。 光:未测定。
BCS分类:Ⅲ类
制剂处方
处方来源:FDA 施贵宝的GLUCOPHAGE处方,规格1g 辅料组成:聚维酮,硬脂酸镁、羟丙纤维素、聚乙二醇 处方来源:Fortmet Andrx Labs LLC 羟丙甲纤维素、硬脂酸镁、聚乙二醇、聚山梨酯80、二氧化钛、聚维酮、十二烷基硫酸钠、黑色氧化铁、三乙酸甘油酯、醋酸纤维素、树蜡
溶出曲线
PMDA溶出曲线
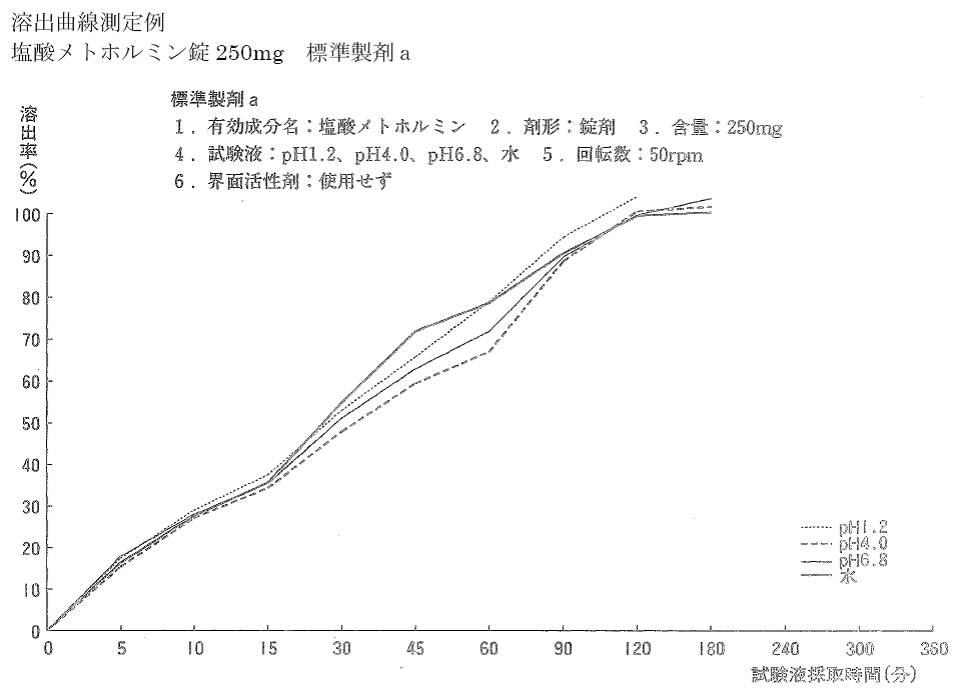
方法:桨板法,以水900ml为溶剂,转速为每分钟50转,120分钟取样(A型)15分钟取样(B型),限度为标示量的85%(A型)或80%(B型)。
溶出度试验条件:桨板法/50转、溶出介质中不添加表面活性剂。
<250mg 片剂 > A型
<250mg 片剂 > B型 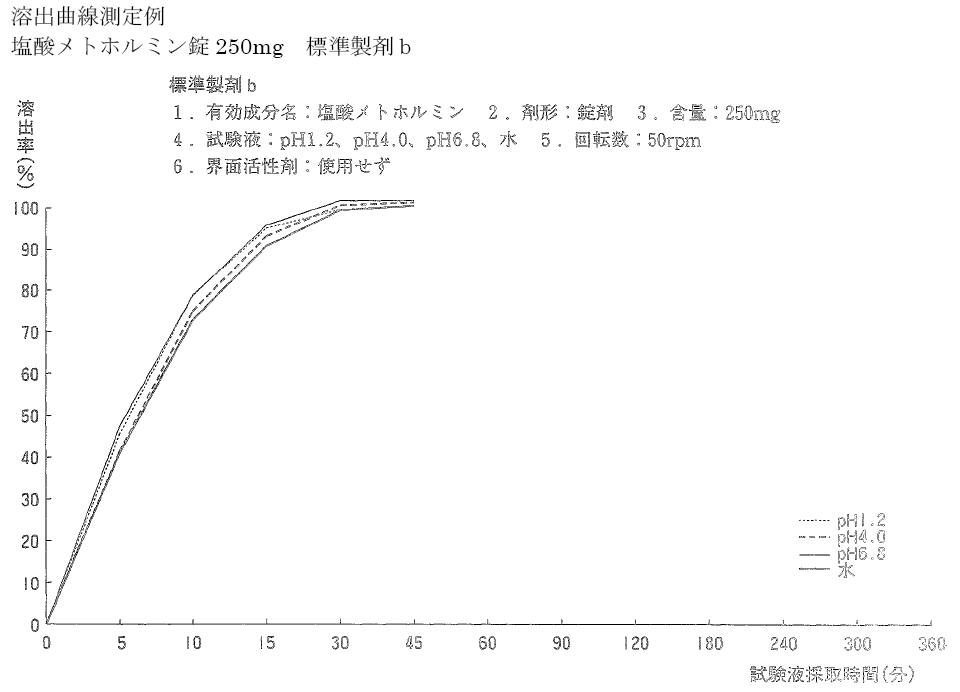
质量标准对比
有关物质
二甲双胍原料 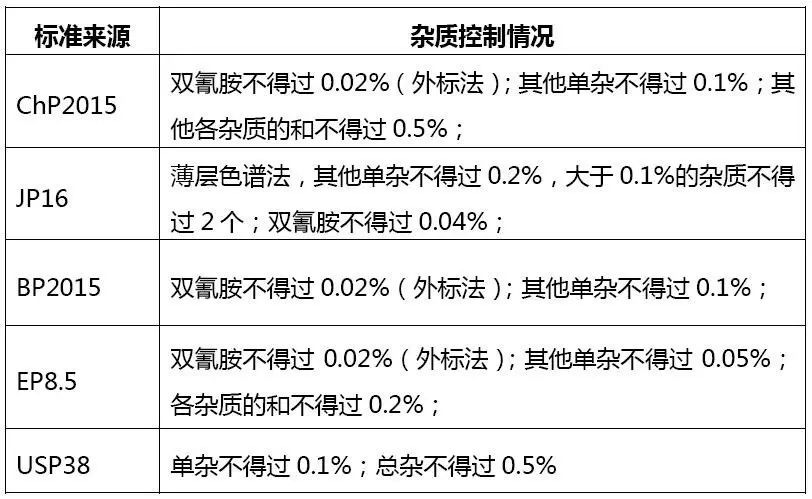
二甲双胍片 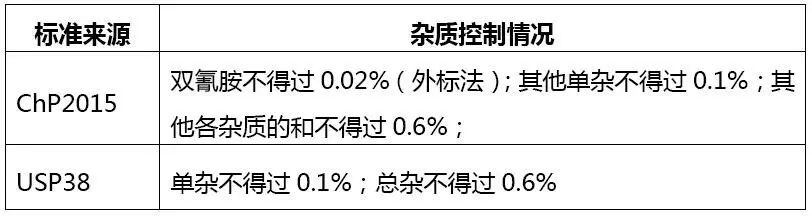
溶出度
盐酸二甲双胍片溶出对比 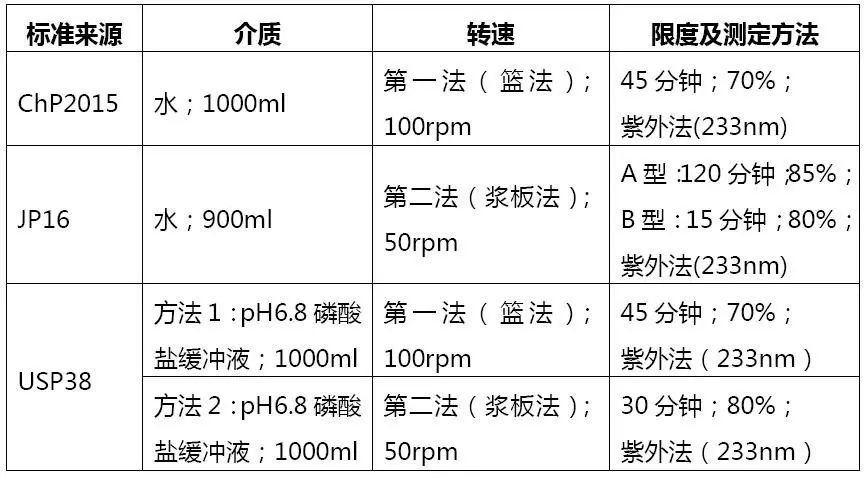
评价:中国药典2015年版介质及溶出相关参数与国外药典不同,比对后可考虑是否修订。
溶出介质设计方案
初步评价:根据普通口服固体制剂溶出曲线测定与比较指导原则,可参考日本溶出度数据库中的四条介质(pH1.2、pH6.8、pH4.0、水)做一致性评价。
深入评价:为确保体内BE等效,视比对情况扩充不同pH介质的溶出。
BE方案及药动学参数
药监文献报道的BE研究方案
试验设计:单剂量、双周期、交叉试验。 剂量:1000mg 试验类型:餐前+餐后 建议方案:二甲双胍片应用240mL 20%的葡萄糖水送服,给药后4h内,间隔15分钟服用60mL葡萄糖水。。 日本橙皮书中BE受试者数:11~28
公开文献报道的BE研究方案及药动学参数
20名健康男性受试者,平均年龄(24.1±2.9)岁,平均身高(171.8±4.7)cm,体重(63.9±8.0)kg,体重指数(BMI) (21.6±4.0)kg/m2。血生化、血常规、尿常规及心电图检查均正常,符合入选标准。受试者均签署书面知情同意书。试验方案经华中科技大学同济医学院伦理委员会批准。
随机,交叉,单剂量口服试验设计。20名健康受试者随机分成2组,每组10 例。受试者禁食12h后,于次日清晨空腹单剂量口服试验或对照药物1.0g,温开水200mL送服,服药2h后方可再饮水,4h后进统一餐。2次试验间隔1周。
于服药前(0h)和服药后0.33、0.67、1、1.5、2、3、4、6、8、10、12、24h取上肢静脉血5.0ml,注入肝素化管中,混匀后离心,转速3000r/min,时间10min,血浆样品置于-80℃冰箱中低温保存。
药动学参数
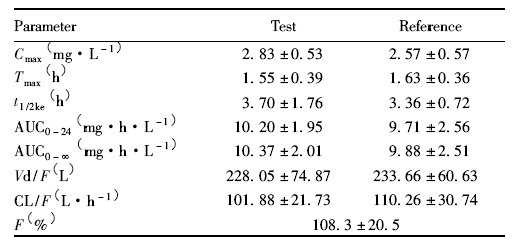
文献中报道的AUC曲线及药动学参数如下所示 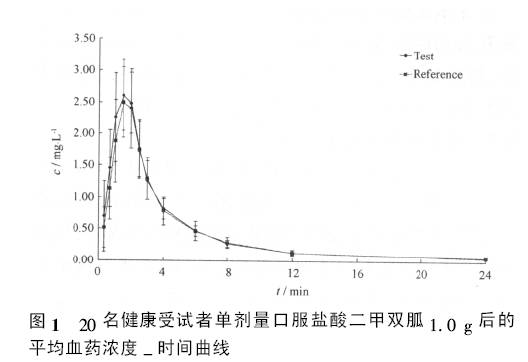
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033