2家国产新药上市本次未获准,收到通知件
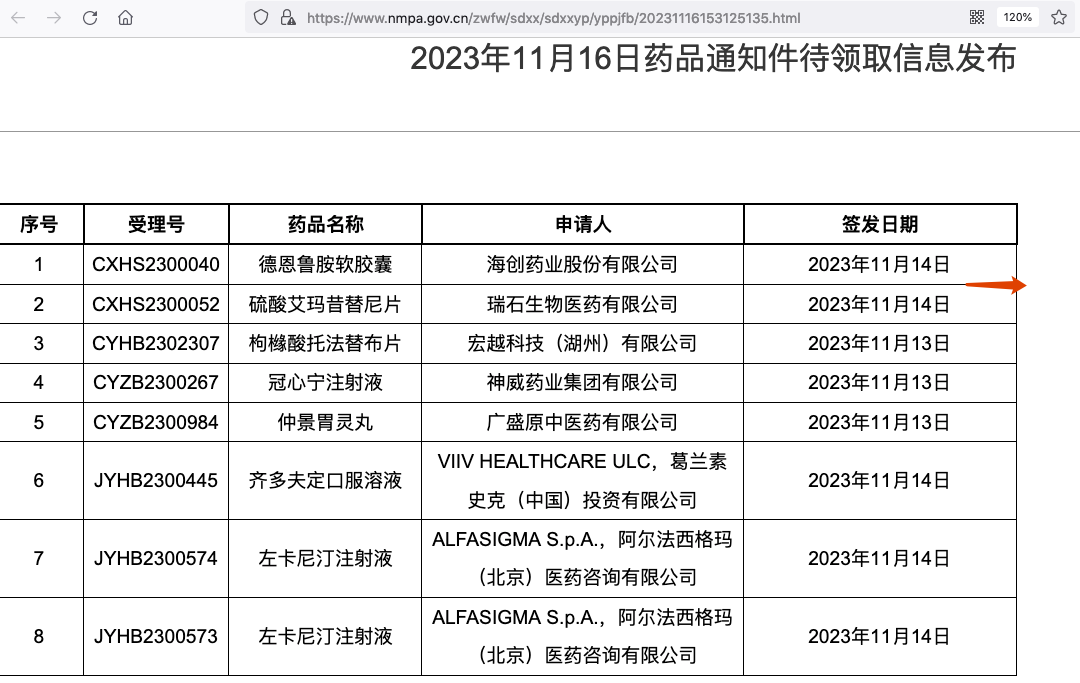
2023年11月16日,国家药品监督管理局(NMPA)新一批的药品通知件待领取信息发布。本次的新药上市申请未获准,不一定是真的被拒绝,不过可以简单窥探一二。
01
海创药业
此前公告,公司提交的氘恩扎鲁胺(曾用通用名:德恩鲁胺)软胶囊上市申请,于2023年03月获国家药品监督管理局(NMPA)药品审评中心(CDE)受理。本品种原料药供应商为“凯莱英医药集团(天津)股份有限公司”(“凯莱英”),其公司于2022年09月在国家药品监督管理局药品审评中心完成原料药登记备案。

近日,海创药业收到原料药供应商凯莱英的通知,其公司已自行提交原料药登记备案的撤回申请。经与多方沟通确认,原料药登记备案撤回将导致本品种制剂申请被动关联撤回,目前CDE的相关流程正在进行中,预计将于2-3周内结束,待流程结束后,公司将尽快完成新药上市申请的重新递交。
 药融云数据www.pharnexcloud.com
药融云数据www.pharnexcloud.com
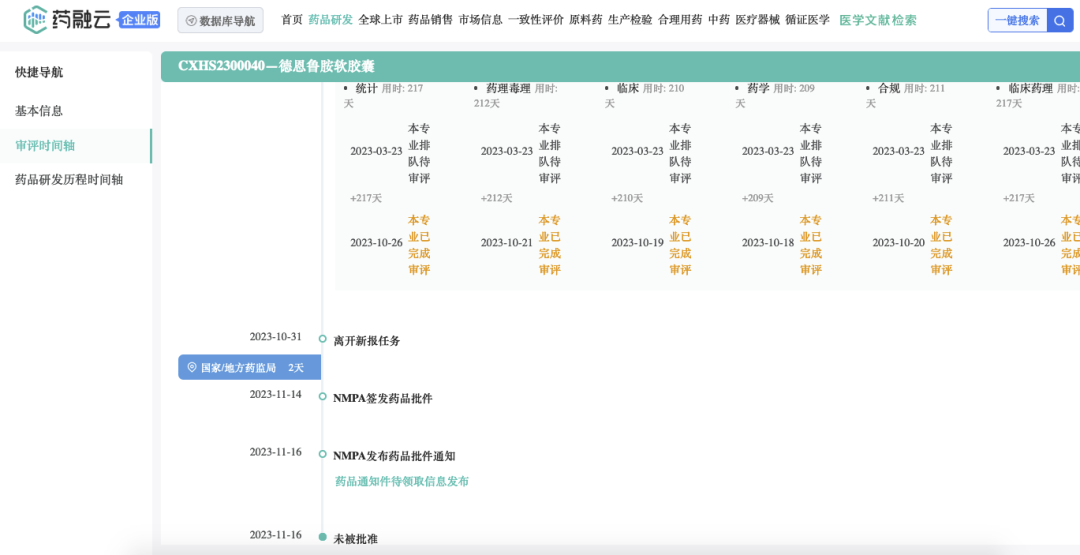
审评进度时间轴
德恩鲁胺(HC-1119软胶囊)是公司自主研发的、治疗转移性去势抵抗性前 列腺癌(mCRPC)的 1 类新药,是第二代雄激素受体(AR)拮抗剂恩扎卢胺的氘代药物,获得国家2018 年“重大新药创制”科技专项支持。
02
恒瑞医药与子公司瑞石生物
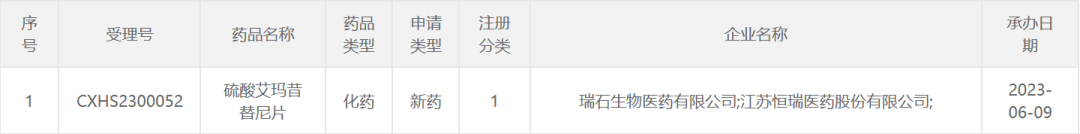
2023年6月,瑞石生物/恒瑞医药的1类新药硫酸艾玛昔替尼片(ivarmacitinib sulfate)的上市申请获国家药监局药品审评中心(CDE)受理。这是国内首个提交上市申请并获受理的国内自主研发的JAK1抑制剂,拟用于青少年及成人中-重度特应性皮炎的治疗。公司当时表示如果该药获批上市,将填补国内企业在中-重度特应性皮炎治疗领域的空白。
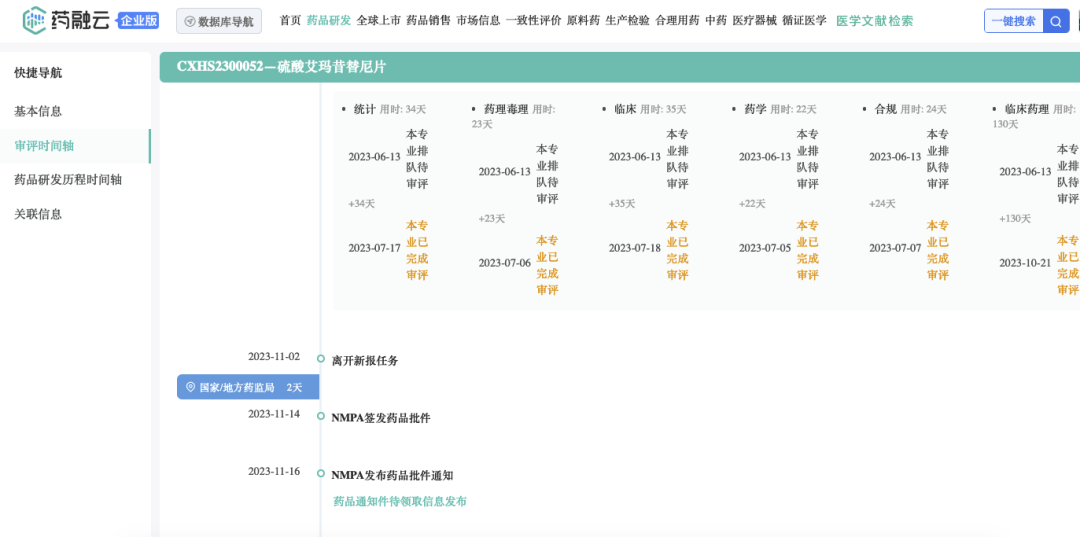
药融云数据www.pharnexcloud.com审评进度时间轴
恒瑞医药2023年8月25日公告,瑞石生物已经撤回了该药治疗中重度特应性皮炎的上市申请,原因是“申报策略调整主动撤回”。不过有投资机构表示,很可能与瑞石生物的大变动(“解散”)/优化或临床试验有关。


不过,该候选分子产品后续在11月3日,递交的新的AD适应症NDA/上市申请获得受理。
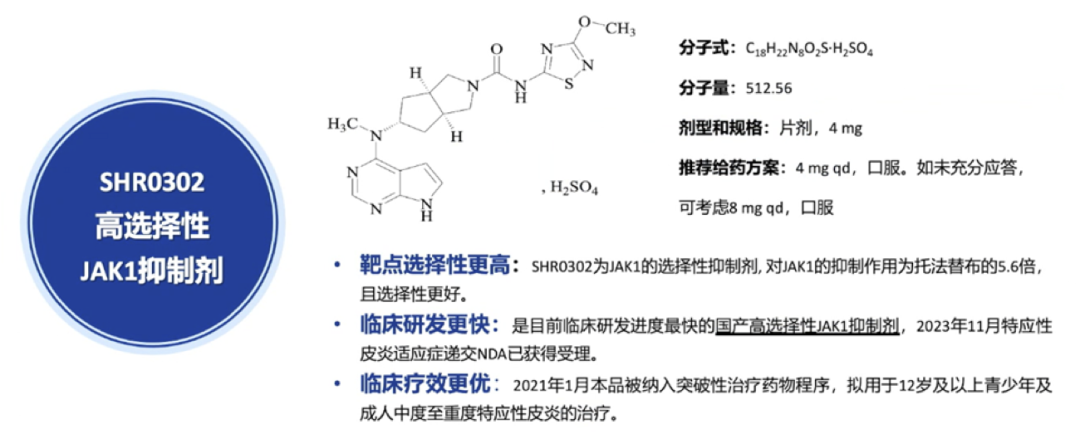
2023年恒瑞医药研发日
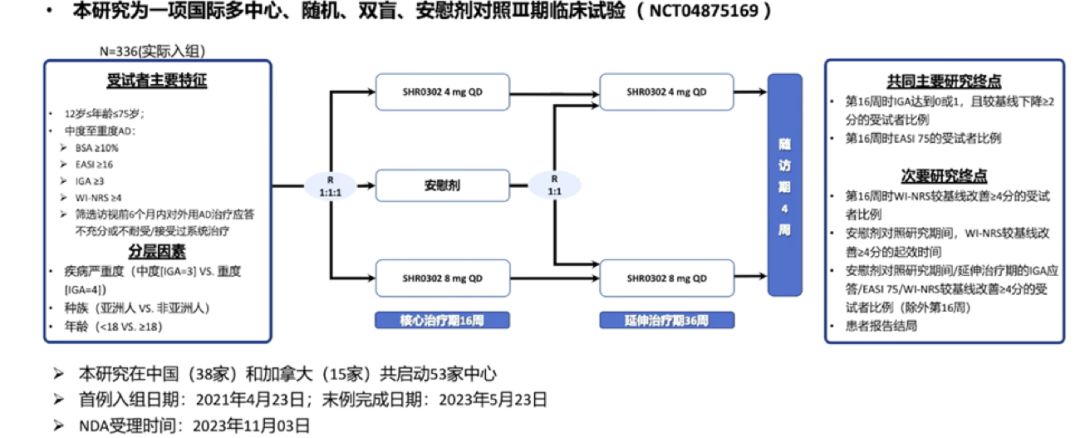
2023年恒瑞医药研发日
附,此前披露的AD适应症数据:
QUARTZ3是一项随机、双盲、安慰剂对照、国际多中心3期注册性临床试验,由北京大学人民医院张建中教授牵头在全球51家研究中心开展,旨在评价艾玛昔替尼单药治疗中重度特应性皮炎患者52周的有效性和安全性。试验共纳入336名12岁及以上中至重度特应性皮炎受试者,随机接受口服每日一次8mg或4mg艾玛昔替尼或安慰剂治疗,完成16周治疗的受试者将进入为期36周的延伸治疗期。
研究达到了预设的共同主要终点,与安慰剂相比,每日一次口服艾玛昔替尼8mg或4mg能够显著改善中度至重度特应性皮炎患者的临床症状,清除皮损并提高生活质量。16周时,艾玛昔替尼8mg、4mg组获得研究者总体评分(IGA)达到0(皮损完全清除)或1(几乎完全清除),且较基线下降≥2分(IGA应答)的受试者比例分别为42.0%和36.3%,湿疹面积与严重程度指数(EASI)较基线改善至少75%(EASI-75应答)的受试者比例分别为66.1%和54.0%,与安慰剂组(9.0%和21.6%)相比,应答率差异均具有显著的统计学意义。
在改善皮肤瘙痒方面,艾玛昔替尼起效迅速,两种剂量组瘙痒减轻的受试者比例早在第4周即与第16周时相似。第16周时,达到最严重瘙痒数字评分改善≥4分(WI-NRS 4)应答的受试者人数(比例)在艾玛昔替尼8mg组和艾玛昔替尼4mg组分别为45(40.2%)和42(37.2%),而在安慰剂组为14(12.6%)。艾玛昔替尼8mg组和艾玛昔替尼4mg组的应答率,较之安慰剂组的差值分别为26.6%和24.6%,差异均有统计学意义。艾玛昔替尼两种剂量均具有良好的耐受性,不良事件的总体发生率与安慰剂组相当,严重不良事件和导致停用研究药物的不良事件的发生率均未增加。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/1VAD4dVIzixEgofPYqrihw)



