暴跌67%!终止三项3期临床试验,小Biotech该何去何从
12月26日,安进宣布,FDA拒绝完全批准Lumakras,用于治疗既往至少接受一次全身治疗的KRAS G12C突变非小细胞肺癌。早在10月美国FDA肿瘤学药物咨询委员会(ODAC)会议上,专家以2 : 8否决了Lumakras的3期CodeBreaK200试验数据的有效性。值得注意的是,2 : 8的反对是对临床设计和实施问题进行讨论的结果,这种低级错误对于MNC来说,是不太寻常的。最后FDA要求安进开展额外的验证性研究,并不晚于2028年2月完成。
12月26日,Milestone Pharmaceuticals宣布,FDA拒绝Etripamil的新药上市申请(DNA),用于治疗阵发性室上性心动过速(PSVT),Etripamil是一种新型钙通道阻滞剂鼻喷雾剂。经初步审查,提交的DNA不够完整,FDA要求该公司澄清3期临床试验中不良事件记录的事件,FDA并没有对不良事件的性质或严重性表示担忧。
以上虽被FDA拒绝,但仍有成功的希望!
而有的公司就没有那么幸运,12月22日,AlloVir宣布终止核心产品Posoleucel 的三项3期临床试验,公司将探讨战略替代方案,可能包括合并、出售、资产剥离、许可或其他战略交易。当日股价暴跌64%,截至目前,股价已跌至0.75美元/股。
Allovir Inc股市情况
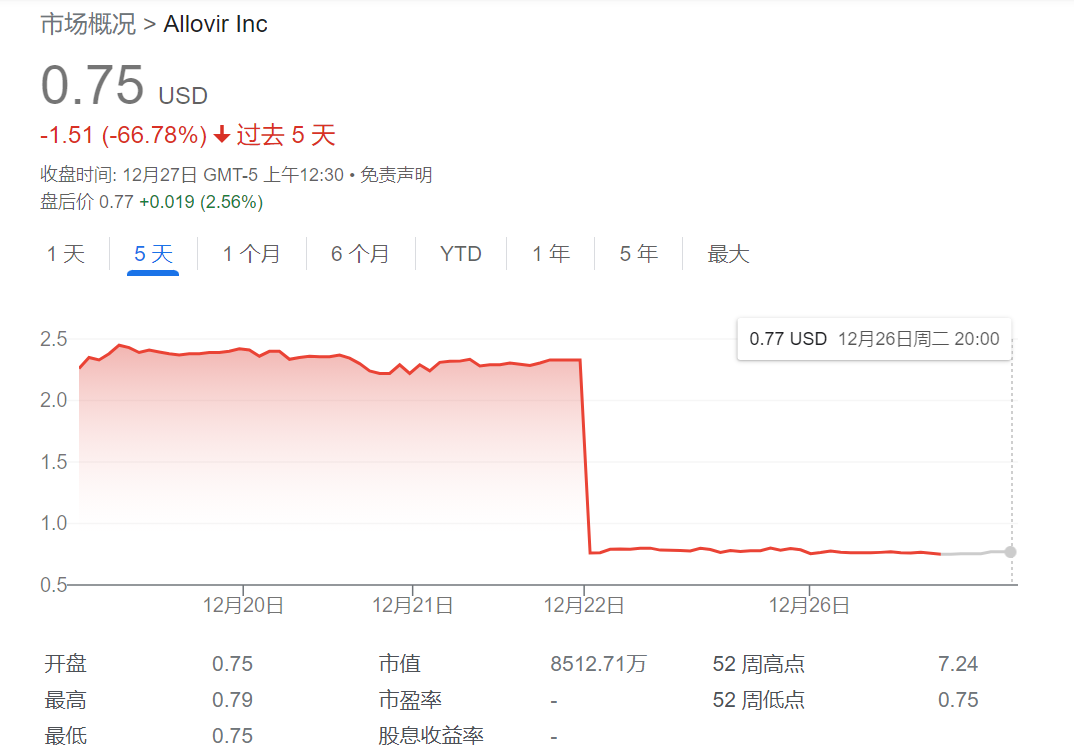
AlloVir在研管线只有3款,其中Posoleucel是该公司的核心产品,也是唯一进入后期管线的产品,2022年7月,吉利德及其他公司投资1.27亿美元支持该产品的开发。
Posoleucel是一种实验性的多病毒特异性T细胞疗法,针对免疫功能低下个体的六种病毒病原体,包括腺病毒(AdV)、BK病毒(BKV)、巨细胞病毒(CMV)、EB病毒(EBV)、人疱疹病毒-6(HHV-6)和JC病毒(JCV)。停止的三项3期临床试验,分别是用于预防多种病毒引起的感染或疾病、治疗病毒相关的出血性膀胱炎(vHC)和治疗腺病毒(AdV)。
Posoleucel研发进度
终止的原因是,数据安全监测委员会(简称DSMBs,是一个专家委员会,负责持续审查临床试验数据,以确保研究受试者的安全性以及数据的有效性和完整性)对数据的审查表明,三项3期研究都不太可能达到其主要终点,唯一值得庆幸的是没有观察到任何安全性问题。
AlloVir首席执行官Diana Brainard表示,“虽然对试验结果感到失望,但对Posoleucel明显的安全性感到鼓舞,将继续分析临床研究数据,以了解可能影响结果或任何明显的亚人群益处变量。”
AlloVir是一家同种异体T细胞免疫疗法公司,于2020 年 7 月上市,最新公告显示,截至2023年9月30日,AlloVir拥有现金、现金等价物和短期投资2.133亿美元,前三季度研发费用支出1亿美元,因此,现有资金至少还能维持AlloVir进行2年的研发。
目前Posoleucel还有一项试验已经处于1b/2期尾声,用于肾移植患BKV感染。据之前的2期随机、安慰剂对照试验结果显示,Posoleucel用于治疗成人肾移植患者的BKV感染,在治疗24周后,治疗组有39%患者的病毒载量减少≥1-log,而安慰剂组的比例为14%。
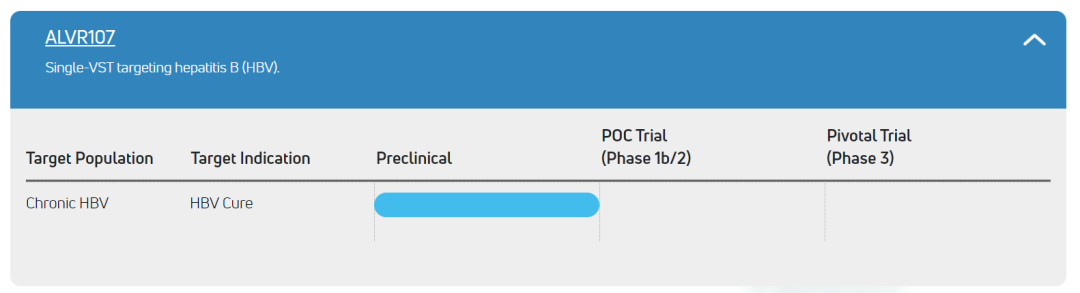
另外,AlloVir还有2款候选药物在研,分别为ALVR106和ALVR107。ALVR106也是多病毒特异性T细胞疗法候选药物,包括人类偏肺病毒(hMPV)、流感病毒(Flu)、副流感病毒(PIV)和呼吸道合胞病毒(RSV)。已在14例干细胞或实体器官移植患者中完成了随机、安慰剂对照1b/2a期试验的A部分,数据将在2024年第一季度科学会议上展示。
ALVR106研发进度
 (图源:AlloVir官网)
(图源:AlloVir官网)
ALVR107研发进度
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/4HzZ0v9aC0iF_CueeUIMUw)



